Клиническая биохимия Агат
МО, г. Балашиха, квартал Щитниково, д. 88А
Пн-Пт с 8:00 до 18:00 (Мск) без перерыва
Пн-Пт с 8:00 до 18:00 (Мск) без перерыва
- Разработка, производство и реализация диагностических наборов, контрольных материалов для клинической биохимии.
- Снабжение лечебных учреждений реактивами, расходными материалами и оборудованием.
- 01. Биохимические наборы реагентов
- 02. Контрольные материалы и калибраторы
- 03. Общеклинические исследования
- 04. Тест-полоски индикаторные
- 05. Коагулология, реагенты для исследования системы гемостаза
- 06. Сыворотки и диагностикумы
- 07. Цоликлоны, реагенты и принадлежности для определения групп крови
- 08. Системы для забора крови и принадлежности
- 09. Дозаторы и наконечники
- 10. Тесты, журналы, индикаторы и принадлежности для стерилизации
- 11. Питательные среды и растворы
- 12. Диски с антибиотиками, системы индикаторные для идентификации микроорганизмов
- 13. Красители для гематологии, цитохимии, микробиологии
- 14. Паразитология и микробиология
- 15. Микроскопы, масло иммерсионное и принадлежности
- 16. Лабораторное оборудование и расходные материалы
- 17. Реактивы для лабораторных исследований
- 18. Лабораторная посуда и изделия из пластмассы
- 19. Лабораторная посуда и изделия из стекла
- 20. Фарфоровая посуда и изделия из фарфора
- 21. Медицинские изделия из силикона и резины
- 22. Литература по лабораторной диагностике
Прайс-лист
Рекламные материалы
-
Листовка "Биологические микроскопы торговой марки Микромед" (в формате pdf)

-
Листовка "Окраска по Цилю-Нильсену-100" (в формате pdf)

-
Листовка "Окраска микроорганизмов по Граму-100 (фуксин)" (в формате pdf)

-
Продукция собственного производства для клинической химии (в формате pdf)

-
Листовка "Лабораторная мебель за 15 дней" (в формате pdf)

-
Буклет на контрольную сыворотку Биоконт-С (в формате pdf)

Референтный метод определения железа в сыворотке крови
(Проблемы гематологии и переливания крови, 1/99, стр.50–53.)
Описан метод определения железа в сыворотке крови человека, рекомендованный Международным комитетом по стандартизации в гематологии в качестве референтного, в современной модификации. В качестве хромогена использован феррозин. Подробно изложена методика определения, особое внимание уделено подготовке отечественных реактивов для достижения необходимого уровня качества. Референтный метод может быть использован для оценки качества разрабатываемых методов определения железа, может быть рекомендован в качестве рутинного анализа.
SUMMARY
Referent method of iron detection in plasma
I.V.Smirnov, G.N.Koltzova, V.V.Gladun
We describe new modification of method of iron detection in human plasma recomended by International Committee for Standardisation in haematology as referent one. Ferrosin was used as chromogene. We report the peculiarities of performing with special emphasis on creating Russian reactives with optimal quantity. Referent method can be used for evaluating of quantity of new-developed methods as well as recommended for routine use.
Содержание железа в сыворотке крови является важным критерием в диагностике ряда гематологических заболеваний, связанных с нарушением метаболизма железа в организме, и, в первую очередь, в дифференциальной диагностике анемий различного происхождения.
В настоящее время в лабораторной практике используется большое число различных методов определения железа в сыворотке крови. Однако Международный комитет по стандартизации в гематологии (ICSH) рекомендует в качестве референтного метода лишь один, который был впервые описан ICSH в 1971 г. [1], затем в 1978 г. [2] и, наконец, в 1990 г. [3]. Предложенные экспертным советом ICSH рекомендации, опубликованные в 1971 г. [1] в качестве экспериментального стандартного метода определения железа в сыворотке крови и сообщенные в 1972 г. [4] детали исследований, проведенных членами этого совета, касались и реагентов и способа определения. Метод был рекомендован для рутинного анализа и реализован, например, в широко известном в России наборе реактивов фирмы LaChema (Чехия). По этому методу 2 мл сыворотки смешивали с 2 мл кислого рабочего раствора, содержащего трихлоруксусную, тиогликолевую и соляную кислоты и выдерживали при комнатной температуре; при этом железо высвобождалось из железосвязывающих белков сыворотки крови и восстанавливалось до двухвалентного состояния. Затем белки удалялись с помощью центрифугирования, а к супернатанту прибавлялся раствор хромогена — динатриевой соли 4,7-дифенил-1,10-фенантролиндисульфоновой кислоты (батофенантролина) в присутствии ацетата натрия для создания в реакционной смеси значения рН 4,5, оптимального для образования окрашенного комплекса, оптическая плотность которого определялась при 535 нм.
В дальнейшем, с учетом последующих исследований членов совета, а также комментариев, полученных от различных организаций и ученых, вышеописанные рекомендации были пересмотрены и опубликованы в 1978г. [2] в качестве ICSH стандарта (ЕР7/1978). Дополнительно было введено нагревание смеси сыворотки с кислым реагентом при 56 оС в течение 15 мин и уменьшение концентрации соляной кислоты с соответствующим уменьшением концентрации ацетата натрия в растворе хромогена.
Через 12 лет ICSH опубликовал [3] вновь пересмотренные рекомендации для измерения сывороточного железа, которые включали замену хромогена и уменьшение объема сывороточной пробы. Ранее было показано, что мононатриевая соль 3-(2-пиридин)-5,6-дифенил-1,2,4-триазин-n,n1-дисульфокислоты (феррозин) и динатриевая соль 3-(2-пиридил)-5,6-бис[2-(5-сульфурил)]-1,2,4,-триазина (ферен) являются более чувствительными хромофорами: феррозин — на 25%, а ферен — на 50%, и, при этом, более дешевыми [5]. Определению железа не препятствовали ни билирубин, ни каротин, а степень погрешности, обусловленная наличием гемоглобина, была аналогична той, что описана для батофенантролина. С рекомендованным восстанавливающим реагентом, тиогликолевой кислотой, наблюдалась очень небольшая погрешность (< 5%) за счет ионов меди, присутствующих в сыворотке. Уменьшение объемов сыворотки и реагентов в 4 раза (от 2 до 0,5 мл) не вредило точности и воспроизводимости, когда в качестве хромогенов применялись феррозин (коэффициент вариации 1,3 %) или ферен (коэффициент вариации 2,1%). Особые требования в этом методе предъявляются к используемым реактивам: содержание железа в них должно быть минимальным, так как от этого зависит оптическая плотность холостой пробы, которая по рекомендациям ICSH не должна превышать 0,015 ед. оптической плотности.
Целью данной работы являлось апробация современного референтного метода определения железа в сыворотке крови человека с использованием реактивов отечественного производства. Особое внимание было уделено очистке реактивов в соответствии с указаниями в рекомендациях ICSH [2].
Материалы и методы
В работе использовались трихлоруксусная, тиогликолевая и соляная кислоты марки «Ч», а также тригидрат уксуснокислого натрия марки «Ч», феррозин (ИЧП «Агат», ныне ООО «Агат-Мед»); сухая контрольная сыворотка «Биоконт С» (ИЧП «Агат», ныне ООО «Агат-Мед»); сыворотка крови доноров.
Стандартный раствор железа с содержанием 500 мкг железа в 100 мл (89,5 мкмоль/л) в присутствии гидроксиламина, Sigma (США).
Определение оптических плотностей растворов проводили на спектрофотометре СФ-46 (ЛОМО, Россия) в кюветах с длиной оптического пути 1 см.
Вода бидистиллированная для проведения всех этапов работ содержала менее 0,2 мкмоль железа в 1 л (1,1 мкг/100 мл). Пригодной является вода, перегнанная в стеклянном оборудовании. Если перегонка воды происходит иначе, она может быть в дальнейшем очищена путем пропускания через деионизатор, содержащий активированный уголь и подходящую ионообменную смолу.
Используемое стеклянное оборудование (пробирки, флаконы, бутылки), освобождали от железа замачиванием в 2 М HCl в течении 6 часов и промывали от кислоты свободной от железа водой.
Соляную кислоту, содержащую менее 5 мкмоль железа на 1 л (28 мкг/100 мл), получали перегонкой в стеклянном оборудовании и первые 20% дистиллята отбрасывались. Собирали и, затем, использовали дистиллят с температурой кипения 106—108° С, представляющий собой азеотропный раствор с плотностью р = 1,1 г/см3 , содержащий 6 моль/л HCl в 1 л [6].
Трихлоруксусную кислоту с содержанием железа менее чем 5 мкмоль/кг (280 мкг/кг), получали перегонкой в стеклянном оборудовании, предварительно освобожденном от железа перегонкой 200 мл соляной кислоты. Оборудование промывалось водой от кислоты и высушивалось перед использованием. При перегонке трихлоруксусной кислоты (200 г) первые 25 г дистиллята отбрасывали. Следующие примерно 150 г с температурой кипения 196—198° С собирали в предварительно тарированные флаконы, которые затем можно хранить в эксикаторе над твердым едким кали.
Тиогликолевую кислоту очищали перегонкой под вакуумом; Ткип =123° С при 35 мм рт.ст. Полученная кислота имела концентрацию 13,4 моль/л (определяли титрованием).
Уксуснокислый натрий очищали от железа следующим образом [7]: 500 г СН3СООNa ? 3Н2О растворяли в дистиллированной воде (общий объем 1 л) при 37° С и отфильтровывали мутный желтоватый раствор через плотный бумажный фильтр до получения прозрачного бесцветного раствора. Такой раствор содержит 3,6 моль/л уксуснокислого натрия.
Приготовление рабочих растворов
1. Депротеинирующий раствор, содержащий 0,6 моль/л трихлоруксусной, 0,4 моль/л тиогликолевой и 1 моль/л соляной кислот готовили из 30 мл перегнанной тиогликолевой кислоты, 165 мл перегнанной соляной кислоты (азеотропная смесь), 100 г перегнанной трихлоруксусной кислоты и воды в мерной колбе на 1 л. Раствор стабилен, по крайней мере, 2 месяца при хранении в темной стеклянной посуде при 2—8° С.
2. Раствор хромогена, содержащий 1,5 М уксуснокислого натрия и 0,5 ммоль/л (0,25 г/л) феррозина готовили из 420 мл очищенного раствора уксуснокислого натрия, 250 мг феррозина и воды до 1 л.
Процедура определения железа в сыворотке:
Опытная проба: К 1 мл депротеинирующего раствора прибавляли 1 мл исследуемой сыворотки и энергично перемешивали вручную или на приборе типа «Vorfex» в течение 60 сек; пробирку накрывали и нагревали 15 мин при 56° С; затем центрифугировали при 3000 об/мин в течение 10 мин, до получения прозрачного супернатанта;
Калибровочная проба: 0,5 мл стандартного раствора железа смешивали с 0,5 мл воды (разведение в два раза) и 1 мл депротеинирующего раствора;
Холостая проба: 1 мл воды смешивали с 1 мл депротеинирующего раствора;
К 1 мл каждого из растворов добавляли по 1 мл раствора хромогена, энергично перемешивали, выдерживали 10 мин и измеряли оптическую плотность опытной и калибровочной пробы при 560 нм против холостой пробы.
Количество железа определяли по формуле:
D сыв
Железо, мкмоль/л = 44,75 * ------------
D станд
Результаты и обсуждение:
В соответствии с последними рекомендациями ICSH [3] для анализа можно использовать 0,5 мл сыворотки и такое же количество реагентов, что в результате дает 1 мл раствора, оптическую плотность которого необходимо определить на спектрофотометре (СФ). В нашей лаборатории, как и в большинстве других отечественных клинических лабораториях, имеется оптическое оборудование, для работы на котором необходимо как минимум 2 мл раствора. Поэтому мы использовали для работы 1 мл сыворотки и соответствующие этому объемы реагентов, что отражено в описании нашей методики определения железа в сыворотке.
Очень важным моментом при анализе является отсутствие гемолиза в сыворотке. Дело в том, что при референтном методе определения железа в гемолизированной сыворотке, железо из гемоглобина частично входит в определяемую величину, значительно ее завышая.
Другим важным моментом при определении железа в сыворотке крови является величина оптической плотности холостой пробы на реактивы. По рекомендациям ICSH она не должна превышать 0,015 е.о.п. [2]. Это ограничение обусловлено стремлением уменьшить возможные ошибки при определении железа в сыворотке крови больных при анемиях и других заболеваниях, связанных с недостатком железа в организме, когда содержание железа в сыворотке очень низкое, например 3—5 мкмоль/л.
Проведенные нами опыты (результаты приведены в табл.1) показали зависимость оптической плотности холостой пробы (D560) от чистоты используемых реактивов, причем при использовании перегнанных реактивов, как описано выше, А560 уменьшается в 10 раз.
Таблица 1
|
Реактивы, использованные для депротеинирующего раствора | ||||
| Трихлоруксусная кислота | Соляная кислота | Тиогликолевая кислота | D 560 | |
| 1 | коммерческая | коммерческая | коммерческая | 0,103 |
| 2 | перегнанная | перегнанная | коммерческая | 0,041 |
| 3 | перегнанная | перегнанная | перегнанная | 0,010–0,015 |
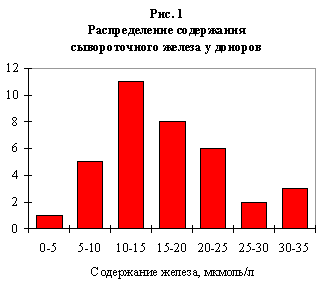
Величина оптической плотности образца, содержащего стандартный раствор железа (500 мкг/дл; 89,5 мкмоль/л) при разведении в два раза, входящая в формулу, по которой вычисляют количество железа составила 0,300 е.о.п. (КВ = 2,5%). Средняя величина содержания железа в сыворотке доноров составила 17 мкмоль/л (n=36), распределенная в интервале 3—32 мкмоль/л (Рис.1). При этом оптическая плотность составляла соответственно 0,114 (0,020—0,214). Коэффициент вариации составлял 3—10% и зависел от вида сыворотки и содержания в ней железа. При анализе контрольной сыворотки «Биоконт-С» с содержанием железа 20—25 мкмоль/л коэффициент вариации составлял не более 5 %.
В методических рекомендациях, как международных [2], так и отечественных [7], стандартный раствор железа предлагается готовить путем растворения точной навески проволоки чистого железа в очищенной соляной кислоте с дальнейшим точным разведением. Нами полагается нецелесообразным приготовление такого стандарта в условиях клинической лаборатории ввиду его трудоемкости и возможности внесения неконтролируемой систематической ошибки. Вполне доступны коммерческие, стандартные и калибровочные растворы железа, как импортного, так и отечественного производства. Как правило, такие растворы содержат гидроксиламин в качестве стабилизатора.
Таким образом, хотя референтный метод ICSH достаточно трудоемкий, он может быть рекомендован в качестве рутинного анализа, но лишь с учетом специфической очистки и подготовки отечественных реактивов. Кроме того, в качестве референтного, он может быть использован для оценки качества других методов определения содержания железа в сыворотке крови.
Литература:
1. Proposed recommendations for measurement of serum iron in human blood. International Committee for Standartdization in Hematology. Brit.J.Haem. 1971, 20(4): 451—453.
2. Recommendations for Measurement of Serum Iron in Human Blood. International Committee for Standartdization in Hematology. Brit.J.Haem. 1978, 38: 219—294.
3. Revised recommendations for the measurements of the serum iron in human blood. International Committee for Standartdization in Hematology. Brit.J.Haem. 1990, 75: 615—616.
4. International Committee for Standartdization in Hematology. Modern Concepts in Haematology (ed.G.Izak; S.M/Ltwis), Academic Press, New York. 1972: 69—160.
5. Thompsen JC, Mottola HC. Kinetics of the complexation of iron (II) with ferrozine. Anal. Chem. 1984, 56: 755—757.
6. Справочник химика, т.III. Москва-Ленинград, изд-во «Химия», 1964:367, 507.
7. Лабораторные методы исследования в клинике (под ред. В.В.Меньшикова), М., Медицина,1987:269—270.
В настоящее время ООО «Агат-Мед» выпускает набор реактивов для определения железа в сыворотке крови «ЖЕЛЕЗО АГАТ».

Производство Агат-Мед
- Биохимические наборы реагентов
- Контрольные материалы и калибраторы
- Красители для гематологии, цитохимии, микробиологии
- Микроскопы, масло иммерсионное и принадлежности
-
Контрольная сыворотка Биоконт-С
-
Масло иммерсионное
-
ГЕМОГЛОБИН-КОНТРОЛЬ


